Comment lutter contre la dénutrition en milieu hospitalier ?
21 novembre 2021
La dénutrition touche plus de 50% des patients atteints d’un cancer ou de la maladie d’Alzheimer en France. Elle peut malheureusement s’aggraver avec la prise en charge thérapeutique. Ceci a pour conséquence d’augmenter la morbidité (c’est-à-dire amplifier la maladie) et la mortalité.
Ces statistiques restent inchangées depuis 30 ans car l’évaluation de l’état nutritionnel du patient est rarement effectuée. Afin de s’assurer de combler ces carences nutritionnels en milieu hospitalier, il est important de pouvoir proposer des suppléments nutritionnels adéquats.1 2
Qu’est-ce que la dénutrition ?
La dénutrition correspond à un déséquilibre entre les apports nutritionnels et les besoins de l’organisme. Ceci peut alors avoir des conséquences importantes, comme le dysfonctionnement de certains organes ou encore la perte de certains tissus et notamment des muscles. Le premier symptôme alarmant est alors l’amaigrissement.2 3
Lorsque la dénutrition devient trop importante, on assiste alors à une cachexie : il s’agit d’un affaiblissement profond de l’organisme caractérisé par une perte importante de masse musculaire, un système immunitaire déficient, et une diminution des capacités cognitives et physiques.4
Comment se fait-il que le nombre de patients dénutris soit aussi élevé ?
Plusieurs éléments peuvent expliquer la dénutrition importante chez les patients, en particulier chez ceux atteints d’un cancer.
D’une part, il n’est pas rare que les patients atteints d’un cancer ne se nourrissent pas suffisamment. En conséquence, les apports sont inférieurs aux besoins de l’organisme. La cause à cela peut être multiple. En effet la maladie ou les traitements peuvent provoquer des dérèglements hormonaux affectant les signaux de la faim, ou avoir un impact psychologique important sur le patient qui pourrait alors perdre en appétit.5
D’autre part, près d’un tiers des cancers touchent des organes liés à la digestion (colon et rectum, foie, pancréas, …) et à l’élimination (système rénal, vessie). Ceci peut alors provoquer un mauvais fonctionnement du système digestif et donc la malabsorption ou la mauvaise utilisation de certains nutriments.3 6
Enfin, dans le cas d’un cancer, la tumeur consomme beaucoup d’énergie au détriment de l’intégrité de l’organisme. Il est donc indispensable que le patient consomme suffisamment d’énergie et de nutriments essentiels afin de ne pas accroître les déficits et les carencesA.4 7
Quelles sont alors les carences et les déficits les plus courants chez ces patients ?
La première carence qui pourra laisser apparaître des effets secondaires visibles est le manque de protéines. Le besoin en protéines est d’environ 0,8g/kg de poids corporel par jour.8 9
En effet, la carence (ou le déficit) protéique est existante dans le cas où l’individu ne consomme pas suffisamment de protéines pour couvrir ses besoins (donc moins de 0,8g/kg/j) ou lorsqu’un acide aminé essentielB est déficitaire. C’est pourquoi les personnes en milieu hospitalier, qui consomment moins d’aliments et/ou les assimilent moins bien, sont très exposés au manque protéique.10
Le déficit d’un ou plusieurs acides aminés essentiels est amplifié dans le cas où l’individu ne consommerait pas suffisamment de protéines de bonne qualité et que les sources ne seraient pas convenablement variées. Pour en savoir plus concernant la définition de la qualité d’une protéine, consultez notre article « Comment définir la qualité d’une protéine ».
Pour synthétiser du muscle, notre corps a besoin de l’ensemble des acides aminés essentiels. Cette synthèse sera alors proportionnelle aux apports nutritionnels de l’acide aminé le plus déficitaire appelé acide aminé limitant. En d’autres termes, si pour l’acide aminé limitant les besoins sont seulement couverts à 30%, alors l’anabolismeC n’atteindra que 30% de son potentiel. Comme l’indique la figure n°1, un déficit d’un unique acide aminé essentiel suffit ainsi pour déséquilibrer la balance protéique.11
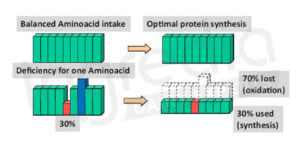
Figure n°1 : Effet du manque d’un acide aminé essentiel sur la synthèse protéique de l’organisme.9
Un déséquilibre chronique des apports protéiques peut entraîner une perte progressive de la masse musculaire accompagnée d’une diminution de la force physique.1 2 4 Mais ce n’est pas le seul risque de la diminution de la masse musculaire. En effet, ceci entraîne également une diminution progressive des fonctions du système immunitaires car ce dernier a besoin d’acides aminés pour fonctionner correctement. Cela entraîne alors une augmentation de la morbidité et du risque d’infection grave, et donc de la mortalité (figure 2).12 13
Ainsi, une nutrition adéquate et surtout un apport suffisant en protéine est vital pour ces patients.
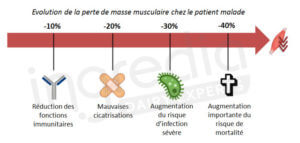
Figure n°2 : Impact de la diminution de la masse musculaire sur le patient malade.12 13
Ne faudrait-il pas mieux consommer davantage de protéines afin de s’assurer de ne manquer d’aucun acide aminé ?
En effet, nous considérons souvent la valeur de 0,8g de protéines par kg de poids corporel par jour. Cependant, pour un patient souffrant d’une maladie comme un cancer, il est recommandé de consommer davantage de protéines. Avec les connaissances scientifiques actuelles, il a été montré qu’une consommation d’au moins 1,2 à 1,6g/kg/j de protéines de haute qualité semblait représenter l’apport idéal pour assurer une santé optimale chez l’adulte malade.2 8 14
Par ailleurs, une étude clinique de 2009 a cherché à évaluer le lien entre la nutrition et la diminution de la mortalité chez des patients gravement malades. Ainsi, il a été démontré qu’une augmentation des apports énergétique d’en moyenne 1034kcal avec 47g de protéines en plus chaque jour permettait de diminuer significativement le risque de mortalité chez les patients dénutris ou en situation d’amaigrissement (figure 3).15
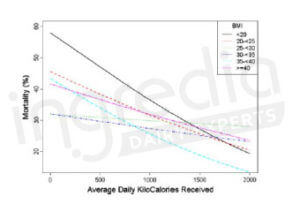
Figure n°3 : Relation entre l’augmentation des apports énergétiques journaliers (dont 18% de protéines) et la mortalité sur 60 jours en fonction de l’IMC (Indice de Masse Corporel).15
De plus, d’autres études ont montré une forte corrélation entre l’augmentation de la consommation de protéines (> 1,2g/kg/j) et l’amélioration de l’état de santé chez les patients malades, s’accompagnant donc d’une réduction et de la mortalité. 7 13 16
Quelle peut être la solution pour assurer convenablement les besoins nutritionnels de ces patients ?
Il existe deux solutions pour mieux couvrir les besoins nutritionnels de ces patients.
La première est simplement d’enrichir l’alimentation. Le but est alors d’augmenter les apports énergétiques et protéiques sans pour autant trop augmenter le volume de la ration. Pour ce faire, différents produits peuvent être utilisés, tel que la poudre de lait (entier, caséines ou whey), le lait concentré entier, le fromage râpé, les œufs, le beurre de cacahuète, la crème fraîche l’huile et le beurre. Ces aliments représentent soit une charge calorique élevée, notamment dans le cas des aliments gras, soit un concentré de nutriments essentiels, surtout dans le cas des œufs et produits issus du lait.17
Malheureusement, il n’est pas rare que l’enrichissement de l’alimentation ne suffise pas à couvrir les besoins du patient, notamment chez les sujets plus âgés.18 Il est alors possible d’envisager une complémentation nutritionnelle orale. On apporte alors des compléments nutritionnels riches en calories et surtout en protéines et micronutriments (vitamines et minéraux) dans l’objectif de lutter contre la malnutrition. Ces produits sont faciles et rapides à assimiler tout en étant adaptés aux goûts du malade : boisson, crème dessert, potage, etc… La Haute Autorité de Santé recommande la prescription de produits hyperénergétiques et/ou hyperprotéinés pour atteindre un apport alimentaire supplémentaire de 400kcal/j et/ou de 30g/j de protéines, le plus souvent avec 2 produits par jour.19 20
Quel type de protéines contiennent ces compléments nutritionnels oraux ?
Ces produits contiennent souvent des caséines micellaires, car ce sont des protéines complètes pouvant répondre aux besoins des personnes dénutris. De plus, elles sont idéales pour la formulation de boissons ou crèmes desserts car elles sont résistantes aux traitements thermiques et permettent de conserver la texture souhaitée au produit.21
Pour plus d’informations, n’hésitez pas à nous contacter.
Auteurs : Rémi Maleterre & Audrey Boulier.
*A [Déficit / Carence] : Un déficit en un nutriment correspond à un apport inférieur au besoin minimal de l’organisme, mais ce manque reste léger et n’a donc pas de conséquences visibles. Alors que dans le cas d’une carence il s’agit d’un manque important d’une molécule à tel point que des effets secondaires surviennent.
*B [Acide aminé essentiel] : Acide aminé que l’organisme n’est pas capable de synthétiser et qu’il est indispensable d’apporter par l’alimentation
*C [Anabolisme] : Synthèse des protéines musculaires.
________________________________________________________________________________________________
[1] Benoist, A. Brouquet (2015). Dépistage de la dénutriton. Nutritional assessment and screening for malnutrition. Journal de Chirurgie Viscérale, 152(1):3-7. Pub February 2015. https://doi.org/10.1016/S1878-786X(15)30002-4
[2] SFNEP (Société Francophone Nutrition Clinique et Métabolisme). « Nutrition chez le patient adulte atteint de cancer ». Recommandations professionnelles de la SFNEP [présentation de novembre 2012]
[3] P. Shetty (2006). Malnutrition and undernutrition. Medicine, 34(12):524-529. Pub December 2006. https://doi.org/10.1053/j.mpmed.2006.09.014
[4] J.M. Argilés (2005). Cancer-associated malnutrition. Eur J Oncol Nurs. 9(2):S39-50. https://doi.org/10.1016/j.ejon.2005.09.006
[5] Cancer Treatment Centers of America. “Malnutrition” [online] https://www.cancercenter.com/integrative-care/malnutrition. Last accessed September 3, 2019.
[6] American Cancer Society: Cancer Facts and Figures 2019. Atlanta, Ga: American Cancer Society, 2019 [online]. https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/annual-cancer-facts-and-figures/2019/cancer-facts-and-figures-2019.pdf. Last accessed September 3, 2019.
[7] H.F.R. da Cunha, E.E.M. da Rocha, M. Hissa (2013). Protein requirements, morbidity and mortality in critically ill patients: fundamentals and applications. Rev Bras Ter Intensiva, 25(1):49-55. Pub January 2013. https://doi.org/10.1590/S0103-507X2013000100010
[8] Poortmans, J.R., Carpentier, A., Pereira-Lancha, L.O., & Lancha Jr., A. (2012). Protein turnover, amino acid requirements and recommendations for athletes and active populations. Brazilian Journal of Medical and Biological Research, 45(10), 875-890. Epub June 06, 2012.https://dx.doi.org/10.1590/S0100-879X2012007500096
[9] Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail (ANSES). (2019) Les protéines : définition, rôle dans l’organisme, sources alimentaires. https://www.anses.fr/fr/content/les-prot%C3%A9ines
[10] D.W. Nixon, S.B. Heymsfield, A.E. Cohen, M.H. Kutner, J. Ansley, D.H. Lawson, D. Rudman (1980). Protein-calorie undernutrition in hospitalized cancer patients. The American Journal of Medicine, 86(5): 683-690. Pub May 1980. https://doi.org/10.1016/0002-9343(80)90254-5
[11] M.F. Holick (2003). Vitamin D: a millennium perspective. J Cell Biochem. 1;88(2):296-307. Pub February 1, 2003. https://doi.org/10.1002/jcb.10338
[12] D.W. Chang, L. DeSanti, R.H. Demling (1998). Anticatabolic and anabolic strategies in critical illness: a review of current treatment modalities. Shock, 10(3):155-60. Pub September 1998.
[13] Frebesenius Kabi. « The Role of Protein in critically ill patients » [online]. https://clinicalnutrition.com.ar/en/the-role-of-protein-in-critically-ill-patients/. Last accessed September 6, 2019.
[14] S.M. Philips, S. Chevalier, H.J. Leidy (2016). Protein « requirements » beyond the RDA : implications for optimizing health. Adv. Physiol. Nutr. Metab. 41(5): 565-572. Epub February 9, 2016. https://doi.org/10.1139/apnm-2015-0550
[15] C. Alberda, L. Gramlich, N. Jones, K. Jeejeebhoy, A.G. Day, R. Dhaliwal (2009). The relationship between nutritional intake and clinical outcomes in critically ill patients: results of international multicenter observational study. Intensive Care Medicine, 35(10):1728-1737. Pub July 02, 2009. https://doi.org/10.1007/s00134-009-1567-4
[16] P.J.M Weijs, S.N. Stapel, S.D.W. de Groot, R.H. Driessen, E. de Jong, A.R.J. Girbes, R.J.M. Strack van Schijndel, A. Beishuizen (2011). Optimal Protein and Energy Nutrition decreases mortality in mechanically ventilated, critically ill patients. Journal of Parenteral and Enteral Nutrition, 36(1):60-68. Pub December 13, 2011. https://doi.org/10.1177/0148607111415109
[17] B. Dorner (2009). Fortify to enhance nutritional value. Today’s Dietitian, 11(7):20. Pub July 2009. https://www.todaysdietitian.com/newarchives/062909p20.shtml
[18] C. Gaillard, E. Alix, Y. Boirie, G. Berrut, P. Ritz (2008). Are elderly hospitalized patients getting enough protein? Journal of the American Geriatrics Society. 56(6):1045-1049. Pub June 02, 2008. https://doi.org/10.1111/j.1532-54152008.01721
[19] I. Bourdel-Marchasson, M. Barateau, V. Rondeau, L. Dequae-Merchadou, N. Salles-Montaudon, J.P. Emeriau, G. Manciet, J.F. Dartiques (2000). A multi-center trial of the effects of oral nutritional supplementation in critically ill older inpatients. Nutrition, 16(1):1-5. Pub January 2000. https://doi.org/10.1016/s0899-9007(99)00227-0
[20] HAS (Haute Autorité de Santé). « Synthèse des recommandations professionnelles (2007) ». Stratégie de prise en charge en cas de dénutrition protéino-énergétique chez la personne âgée. [online]. https://www.has-sante.fr/upload/docs/application/pdf/synthese_denutrition_personnes_agees.pdf. Last accessed September 4, 2019.
[21] Ingredia, Prodiet Fluid. The Innovative Micellar Casein dedicated to high protein beverages. [online] https://www.prodiet-fluid.com/. Last accessed September 4, 2019.